-
Články
Top novinky
Reklama- Vzdělávání
- Časopisy
Nové číslo
- Témata
Top novinky
Reklama- Videa
- Podcasty
Nové podcasty
Reklama- Práce v oboru
Doporučené pozice
Reklama- Praxe
Top novinky
ReklamaKam směřuje vývoj nových antituberkulotik?
Část 2 – Hodnocení in vitro
Where does the development of new antituberculotics go?
Part 2 – In vitro evaluationThe present paper is a continuation of a publication of 2012 (Čes. a slov. Farm. 2012; 31, 150–158). It is oriented at the evaluation of potential antituberculotics in vitro, which is the most widely used approach to testing. The paper is based on the information from Chemical Abstracts 2011–2013. It is a selection from nearly three thousand items of information intended to help researchers. The greatest attention is paid to the multiresistant strains of Mycobacterium tuberculosis. In vitro evaluation for the development of new drugs is of great importance, but it is just the first stretch of the road to new medicinal drugs.
Keywords:
antituberculotics, in vitro evaluation, multiresistant strains
Autoři: Karel Waisser
Působiště autorů: Univerzita Karlova v Praze, Farmaceutická fakulta v Hradci Králové
Vyšlo v časopise: Čes. slov. Farm., 2014; 63, 13-16
Kategorie: Přehledy a odborná sdělení
Souhrn
Článek pokračuje v publikaci z roku 2012 (Čes. slov. Farm. 2012; 31, 150–158). Je orientován na hodnoceni potenciálních antituberkulotik in vitro, což je nejčastější přístup testování. Článek je založen na informacích z Chemical Abstracts z let 2011–2013. Je to výběr z téměř 3000 informací pro pomoc výzkumníkům. Největší pozornost je věnována multirezistentním kmenům Mycobacterium tuberculosis. Hodnocení in vitro pro vývoj nových léčiv je velmi důležité, avšak je to jen první část cesty k novým léčivům.
Klíčová slova:
antituberkulotika, hodnocení in vitro, multirezistentní kmenyÚvod
V předešlé práci jsme ukázali, kam směřuje vývoj nových antituberkulotik1) . Dříve se předpokládalo, že okolo roku 2000 tuberkulóza zanikne ve vyspělé části světa. Tehdy vycházelo méně než 1000 prací ročně. Potenciální antiruberkulotika tehdy bylo možné registrovat a roztřídit podle jejich struktury. Tak vznikla série přehledných referátů pod názvem „Pokroky ve vývoji nových antituberkulotik za posledních 15 let“2–8), která udávala přehled výzkumu tehdejší doby. Prognóza o zániku onemocnění nebyla však správná. Pro nesmírný nárůst počtu onemocnění se vývoj antituberkulotik stal jedním ze stěžejních zájmů farmaceutického výzkumu. Změnu způsobil vznik rezistentních kmenů, na růstu onemocnění se podílela také nemoc HIV a klesající imunita populace léčené od dětských let antibiotiky. Evidence růstu vědeckých prací je uvedena v předchozím sdělení1). Rostoucí počet vědeckých prací dále pokračuje. Pouze za rok 2012 jich bylo uveřejněno více než 3400. Za současné situace již není možné k registraci prací přistupovat dřívějším způsobem.
Hodnocení v České republice a Slovenské republice
V předchozím referátu jsme zcela ignorovali hodnoceni in vitro, které je nejrozšířenější (ročně čítá několik tisíc sdělení). K hodnocení postačí běžně vybavená mikrobiologická laboratoř. Je to prakticky jediný způsob používaný v České republice a ve Slovenské republice. Sledování antimykobakteriální aktivity se provádí na živných kapalných nebo pevných půdách (v České republice a v Slovenské republice se nejčastější používá Šulova kapalná půda, která je dostupná komerčně). Při sledování se hledají minimální inhibiční koncentrace látek (MIC), což jsou koncentrace, které způsobí inhibici růstu sledovaných bakterií. Odečtu předchází doba inkubace za standardních podmínek, nejčastěji v případě pomalu rostoucích mykobakterií je to doba 14 dní (méně často 1 týden) při 37°C. Mikrobiologové vždy postupují tak, že roztok nejvyšší koncentrace studované látky ředí postupně v určitém poměru (např. 1 : 1 nebo 1 : 2 či 1 : 3). Za minimální inhibiční koncentraci považují hraniční hodnotu intervalu v použité stupnici ředění. V našich laboratořích používáme molární koncentrace (μmol/l), většina laboratoří převážně používá váhové koncentrace (μg/cm3). Náš způsob je vhodnější pro následné studie QSAR, protože vystihují efekty stejných počtů molekul. Při váhových koncentracích některá pracoviště provádějí následné přepočty na molární koncentrace. Je to však správné pouze ve skupinách látek podobné molekulární hmotnosti, jinak rozdíly molární hmotnosti nepříznivě ovlivní výpočet. V QSAR studiích se vždy pracuje s log MIC nikoliv s vlastními MIC. Mikrobiologové pokládají hraniční hodnotu intervalu za vlastní minimální inhibiční koncentraci. Lze však předpokládat, že vlastní inhibiční koncentrace se nachází uvnitř intervalu odpovídajícímu postupu ředění. Lze dokázat, jak je velký tento interval, jehož velikost závisí na způsobu ředění. Velikost tohoto intervalu lze vypočítat9–11). Pro postup ředění 1 : 1 v logaritmické stupnici je 0,3. V našich studiích převážně spojujeme hodnocení antimykobakteriální aktivity se studiemi QSAR. Studie QSAR poskytují perspektivu strukturních variací.
Z jiných, méně běžných způsobů vyjádření antimikrobiální aktivity je to průměr zóny na pevném mediu a nebo % inhibice.
V další části referátu jsme se snažili ukázat nejdůležitější práce. Dnes je hlavním zaměřením hledání látek proti multirezistentním kmenům Mycobacterium tuberculosis.
Antituberkulotika při kultivacích in vitro
V České republice a Slovenské republice se do současné doby hodnocení provádí in vitro. Je to nejčastější a nejlevnější způsob. K vývoji léčiva je třeba ještě mnoho dalších kroků. Snad proto se nedostala v České republice a Slovenské republice žádná naše antituberkulotika do praxe, i když zde jsou početné výzkumné skupiny. V současné době se poslední děkan Farmaceutické fakulty UK v Hradci Králové (prof. A. Hrabálek) snaží dovést výzkum do perspektivní fáze. Ve spolupráci s Centrem biologické ochrany v Těchoníně v Orlických horách bude výzkum nejúspěšnějších látek prováděn na zvířatech (in vivo).
V našem článku z tisíce prací o hodnocení in vitro potenciálních antituberkulotik jsme dali přednost sdělením zaměřeným na potenciální léčiva proti multirezistentním kmenům. Tím končíme studii, která začala v předchozím sdělením1). Multirezistentní kmeny M. tuberculosis jsou nejnebezpečnější mykobakterie. Onemocnění často mají fatální konec. Minulé sdělení bylo věnováno různým metodám výzkumu (hodnocení in vivo, QSAR, metody opírající se o biochemické pochody v mykobakteriích) a zcela záměrně bylo vynecháno hodnocení in vitro1). V této části chceme tento nedostatek odstranit. Zaměřili jsme se na pochody in vitro a zvláštní pozornost jsme věnovali jejich orientaci proti multirezistentních kmenům.
Protituberkulózní aktivita thiosemikarbazonů je známá dlouho. V poslední době byla u některých derivátů nalezena aktivita proti multirezistentním kmenům12). Studie ukazuje, že by se jim měla ještě věnovat pozornost. Na obrázku 1 R1 je H nebo CH3, R2 je fenyl, substituovaný fenyl, substituovaný furyl nebo ethyl.
Obr. 1. Thiosemikarbazony účinné proti multirezistentním kmenům 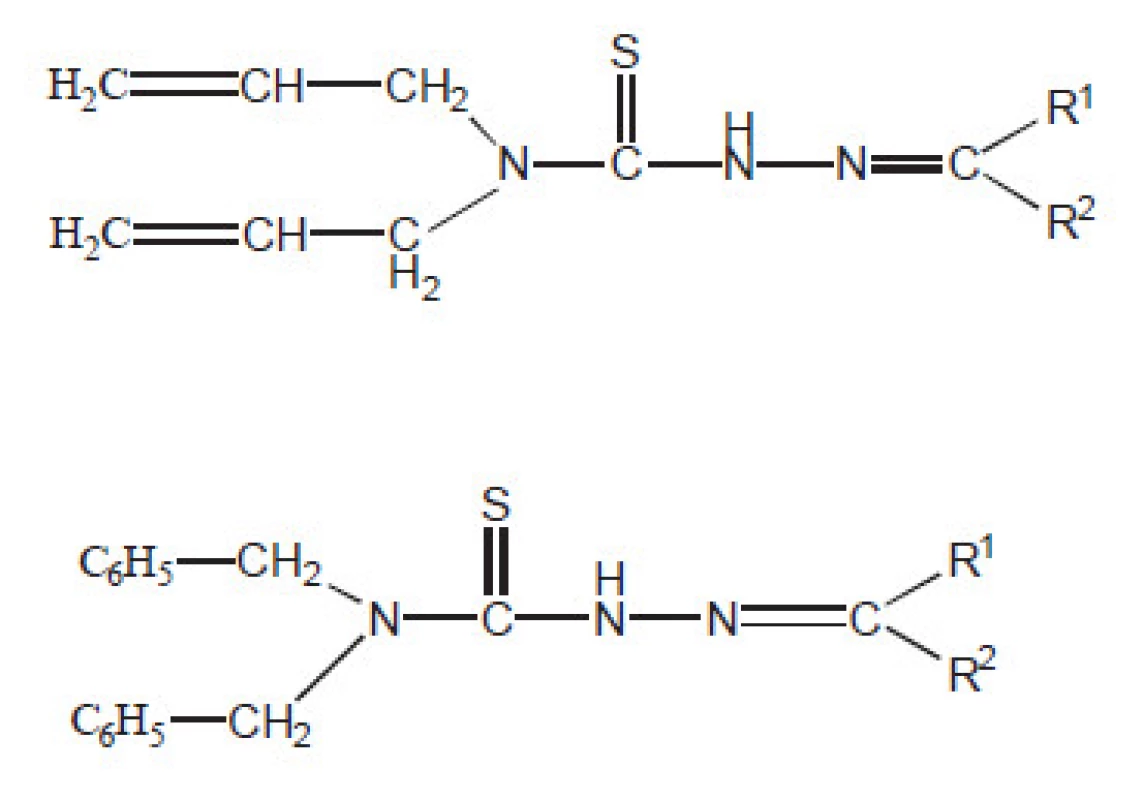
V naší pracovní skupině jsme studovali aktivitu isothiosemikarbazonů.
Častými studovanými sloučeninami pro aktivitu vůči multirezistentním kmenům byly heterocykly. 2,5-disubstituované oxadiazoly byly účinné i vůči extrémně rezistentním kmenům (XDR)13) (obr. 2).
Obr. 2. Příklad účinného 2,5-disubstituovaného oxadiazolu 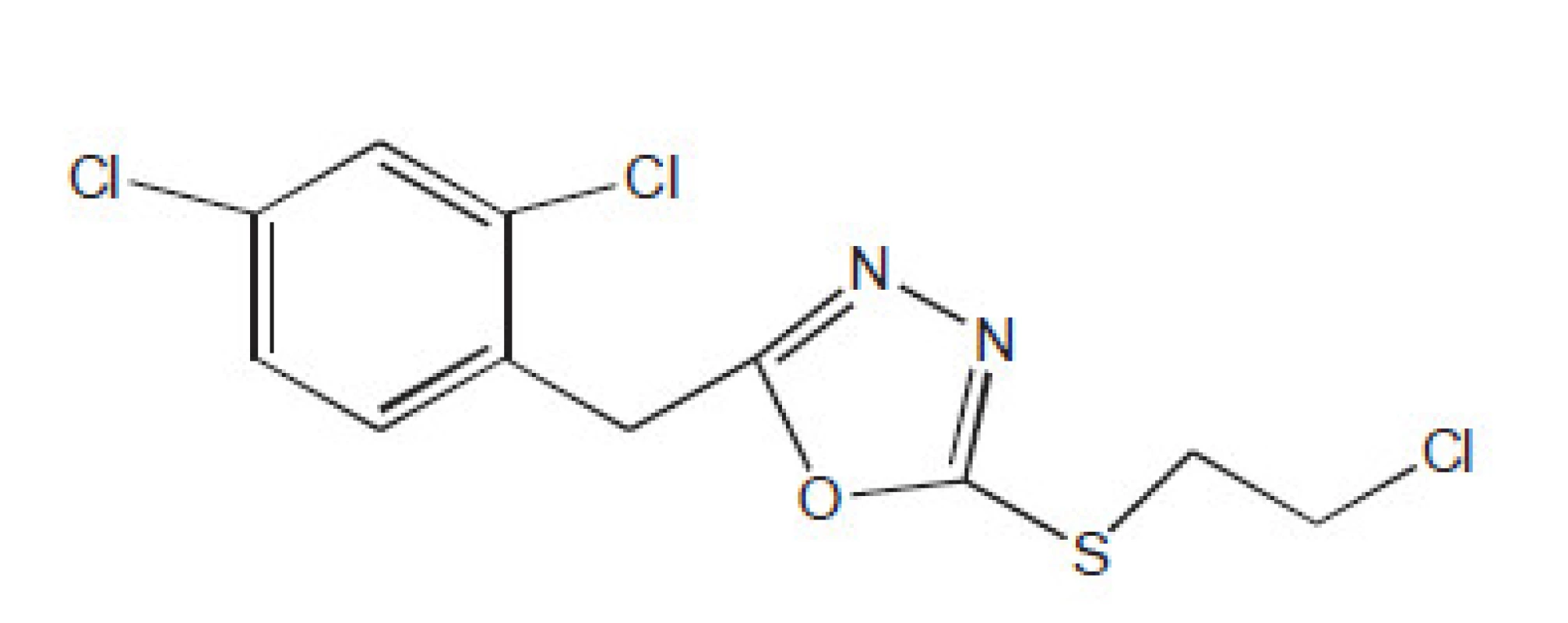
Naproti tomu deriváty 1,5-dimethyl-2-fenyl-4-([-5-arylamino)-1,3,4,-oxadiazol-2-yl]methylamino)-1,2-dihydro-3H-pyrazol-3-onu (obr. 3) nejsou považovány za látky proti MDR kmenům, i když působí proti rezistentním kmenům vůči INH14). Aby byly látky řazeny do skupiny sloučenin působících proti multirezistentním kmenům řady MDR, muselo by být zjištěno působení také proti kmenům rezistentním k rifampicinu.
Obr. 3. Struktura nejúčinnější látky ve sledované skupině derivátů 1,5-dimethyl-2-fenyl-4- ([5-(arylamino)-1,3,4,-oxadiazol-2-yl]methylamino)-1,2-dihydro- 3H-pyrazol-3-onu ![Struktura nejúčinnější látky ve sledované skupině derivátů 1,5-dimethyl-2-fenyl-4- ([5-(arylamino)-1,3,4,-oxadiazol-2-yl]methylamino)-1,2-dihydro- 3H-pyrazol-3-onu](https://pl-master.mdcdn.cz/media/cache/media_object_image_small/media/image/8599099597c61ebbece2cf5a4765171a.jpg)
Ve vývoji látek aktivních proti multirezistentním kmenům se uplatňovaly i některé heterocyklické sloučeniny se šestičlenným heterocyklem. Jako příklad si uvedeme deriváty 4-(substituovaného benzylsulfanyl)pyridin-2-karboxamidu (obr. 4)15).
Obr. 4. Deriváty benzylsufanylpyridin-2-karboxamidu 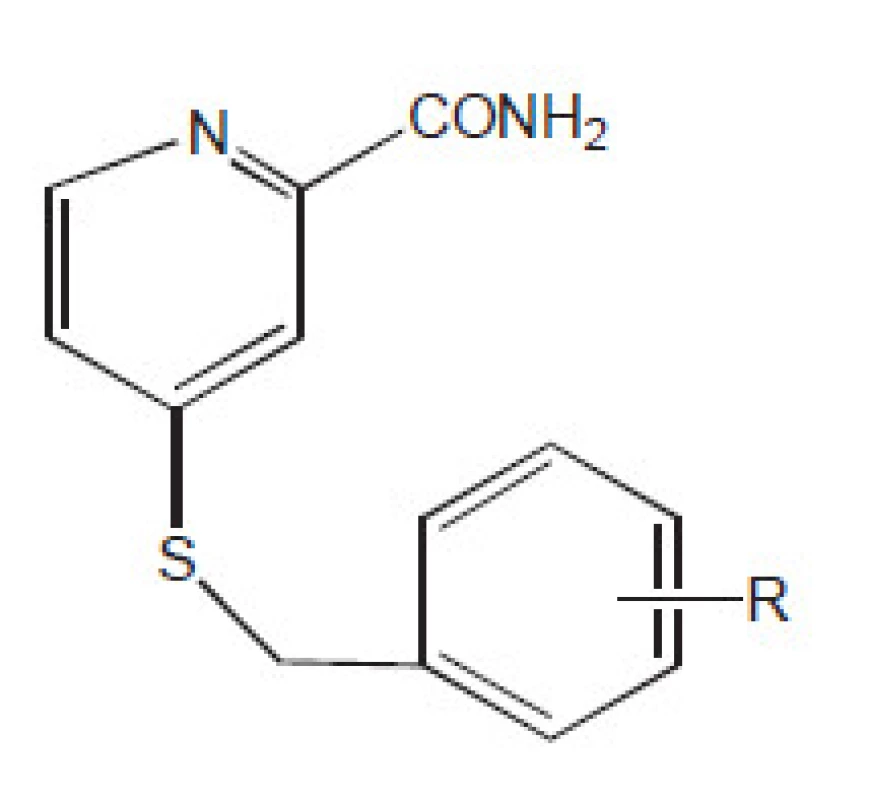
Skupinu R tvořily H, 3-Cl, 4-Cl, 3-F, 4-F, 3-Br, 4-Br, 3-CH3, 4-CH3, 3-CF3. 4-CF3,3-CN, 3-OCH3, 4-NO2, 3,5-(NO2)2. Je to příklad přístupu, kde se syntetizuje skupina látek a hledá se směr k nejúčinnější.
Uvedeme si další příklad složitějších sloučenin (obr. 5 a 6)16). Tyto studie jsou však hodnotnější, protože po hodnocení in vitro přistupuje k hodnocení in vivo. Podobné studie nebyly v České a Slovenské republice po odchodu Odlerové z Ústavu preventivného lekárstva možné provést.
Obr. 5. Příklad spojení studie in vitro a in vivo. R je o-OH, p-OH, o-OCH<sub>3</sub> , p-OCH<sub>3</sub> , p-N(CH<sub>3</sub>)<sub>2</sub> , o-COOH, m-NO<sub>2</sub>, o-NO<sub>2</sub>, o-OH a současně p-OCH<sub>3</sub>, p-Cl, o-Cl, H, furyl, CH=CHAryl 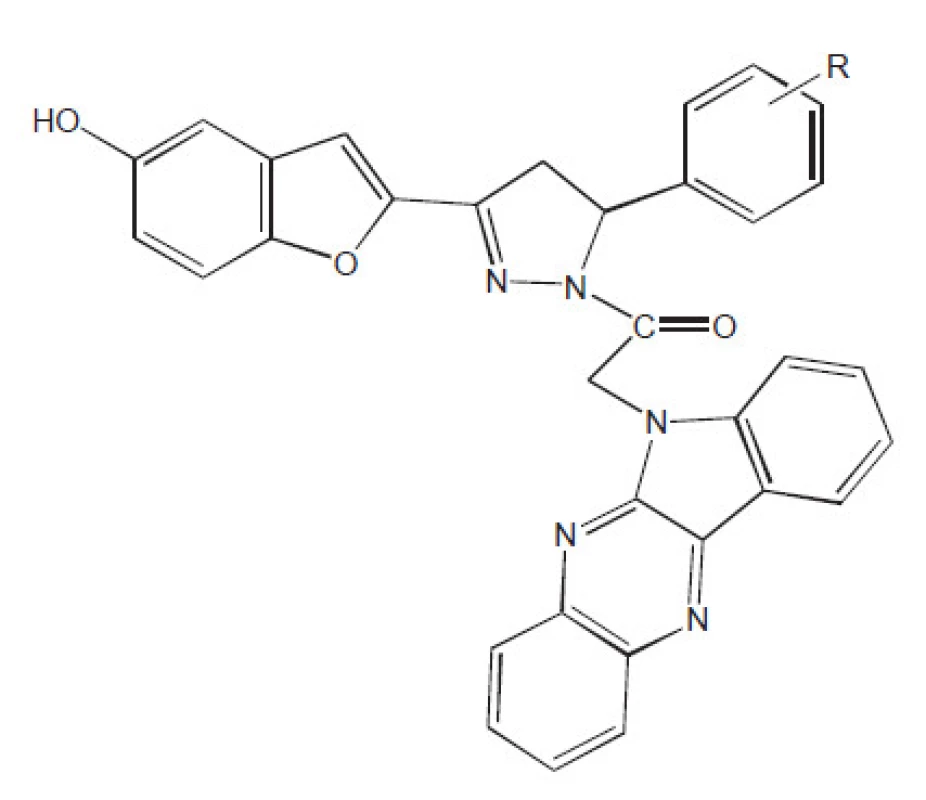
Obr. 6. Antimykobakteriálně aktivní hydrazony (aktivní vůči MD). Skupina je velmi početná. Jako substituenty obsahují řadu různých strukturních částí. 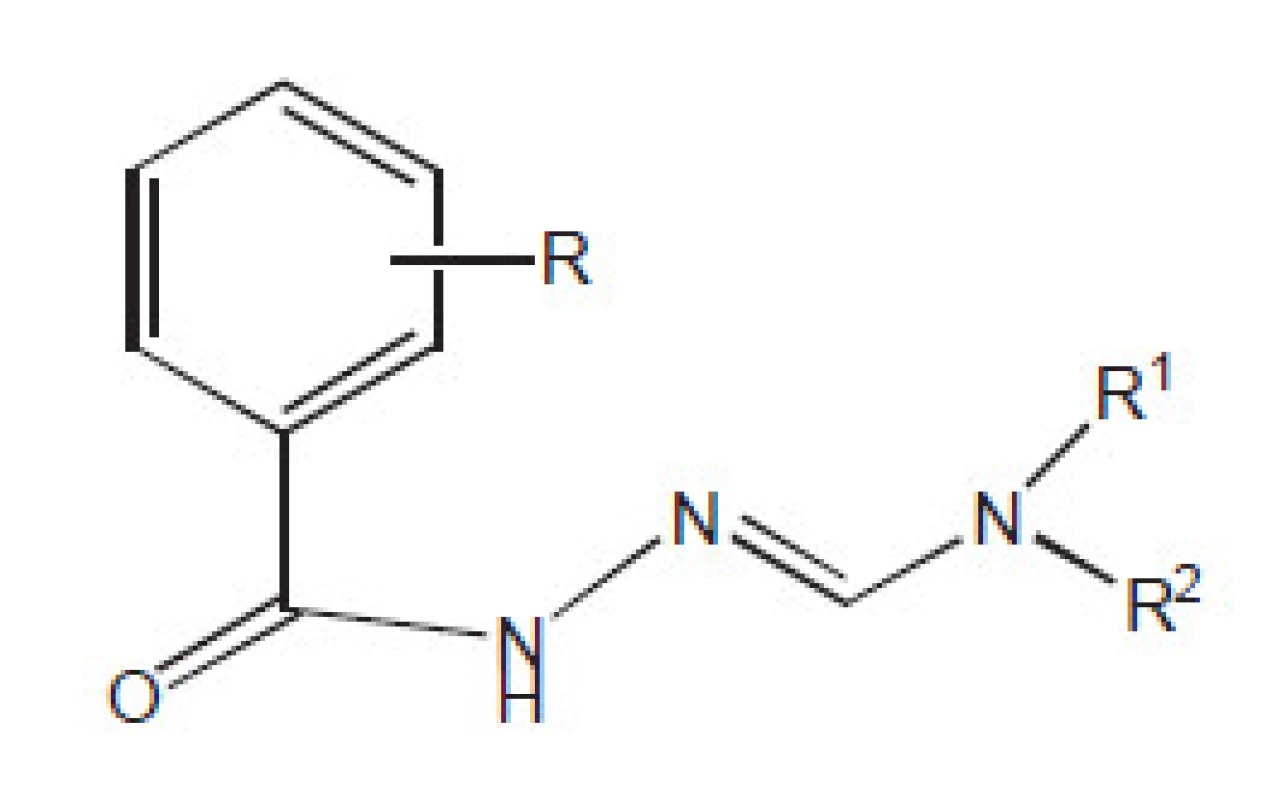
Z uvedených ukázek je vidět, že se jedná o látky rozličných struktur, od velmi jednoduchých, po značně složité, u kterých jsou úspěchy spojeny s náročnými syntézami18).
Pohled na výzkum Farmaceutické fakulty Univerzity Karlovy
Výzkum nových potenciálních antituberkulotik na Farmaceutické fakultě UK má dlouhou tradici. Tématika navázala na předchozí studie z Farmaceutické fakulty UK v Bratislavě a lze tedy říci, že v Hradci Králové uvedená tématika existuje již od vzniku fakulty v roce 1969. Kromě období, kdy hodnocení prováděla Odlerová, vycházely studie pouze z testů prováděných in vitro. V antimykobakteriálním hodnocení se střídaly různé týmy, např. Státní zdravotní ústav v Praze a Regionální zdravotní ústav v Ostravě. Poslední pracoviště bylo spojeno se jménem Kaustová. V současné době hodnocení in vitro látek proti multirezistentním kmenům provádí J. Stolaříková. Výstupem bývala publikační sdělení ve převážně významných vědeckých časopisech, která jsou často citována. Publikovaná sdělení nelze však již patentově chránit. Význam studií byl proto jen teoretický. V posledních letech testy bývaly zaměřeny i na multirezistentní mykobakterie. Na Farmaceutické fakultě v Hradci Králové probíhaly návrhy struktur a syntetické přípravy látek. Zaměření na multirezistentní kmeny mykobakterií je většinou spojeno se jmény Vinšová, Vávrová, Hrabálek, Klimešová a Krátký. Uvádím jen některé odkazy na práce uveřejněné v poslední době17, 19). Vinšová a Krátký jsou autory monografie o vývoji multirezistentních mykobakterií20).
Omezený přístup na hodnocení in vitro vysvětluje, proč se žádná ze syntetizovaných látek v Hradci Králové neprosadila do praxe. Byla však podána řada československých a českých patentů. Tuto situaci chce změnit bývalý děkan fakulty (prof. A. Hrabálek). Dohodl se s Centrem biologické ochrany o hodnocení nejvýznamnějších látek přístupem in vivo (na pokusných zvířatech) a stanovení i toxicity sloučenin. Na tuto spolupráci dostal i finanční dotaci.
Závěr
Na závěr článek uzavírá odpověď na otázku, kam směřuje vývoj současných antituberkulotik. V minulém sdělení jsme uvedli nové metodiky a záměrně jsme vynechali hodnocení in vitro (pro rozsáhlé zastoupení). V posledních letech je výzkum směrován proti multirezistentním mykobakteriím. Multirezistentní bakterie označované MDR jsou rezistentní vůči nejdůležitějším protituberkulózním léčivům, INH a rifampicinu. Pokud jsou dále také rezistentní i proti fluorovaným chinolinům, označují se XDR (extrémně rezistentní). Byl nalezen kmen vzdorující všem soudobým léčivům, označuje se TDR (totálně rezistentní kmen). Na onemocnění vyvolané těmito bakteriemi se převážně umírá. Při sledování směru vývoje výzkumu musíme přihlédnout i k tomuto faktu. Lze však říci, že hodnocení in vitro je úvodem ke studiím. Od uzavření laboratoře Odlerová nebylo v České a ve Slovenské republice možné dále postupovat. Nyní se Farmaceutická fakulta UK v Hradci Králové snaží situaci zlomit a umožnit vývoj nových léčiv. Přehled ukazuje, že katedra má pod vedením A. Hrabálka mnoho vyspělých pracovníků, kteří pracují ve významném směru vývoje antituberkulotik. Lze ještě dodat, že i český patent je bezcenný, protože látka je veřejně přístupná pro celý svět kromě České republiky, a patentování látek celosvětovým (nebo evropským) patentem je velice nákladné. Rozšíření českého patentu na evropský nebo světový je možné pouze do jednoho roku po přijetí českého patentu. Vývoj nového léčiva trvá přibližně 10 let. Největší náklady připadají na farmakologii s prokázáním nezávadnosti preparátu. Vývoj často vyžaduje zahraničního sponzora. Můžeme jen přát kolektivu prof. Hrabálka, aby dosáhl úspěchu. Tímto referátem končí přehled studií o vývoji látek proti tuberkulóze. Věříme, že budoucnost v České republice bude patřit prof. Hrabálkovi a jeho spolupracovníkům.
Střet zájmů: žádný.
Došlo 6. prosince 2013
Přijato 18. prosince 2013
prof. RNDr. Karel Waisser, DrSc. (∗)
Univerzita Karlova v Praze, Farmaceutická fakulta v Hradci Králové
Heyrovského 1203, 500 03 Hradec Králové
e-mail: waisser@faf.cuni.cz
Zdroje
1. Waisser K. Kam směřuje vývoj antituberkulotik? Čes. slov. Farm. 2012; 61(4), 150–152.
2. Waisser K., Holý P., Bureš O. Pokroky ve vývoji nových antituberkkulotik ze skupiny derivátů pyridinu. Čes. a slov. Farm. 2000; 49(5), 211–220.
3. Waisser K., Holý P., Bureš O. Pokroky ve vývoji nových antituberkulotik ze skupiny monocyklických šestičlenných heterocyklických sloučenin o více atomech dusíku. Čes. slov. Farm. 2000; 49(6), 268–277.
4. Waisser K., Bureš O., Holý P. Pokroky ve vývoji nových antituberkulotik ze skupiny ortokondenzovaných heterocyklických sloučenin. Část 1. Látky obsahující v šestičlenném kruhu jeden heteroatom. Čes. slov. Farm. 2001; 50(4), 159–165.
5. Waisser K., Bureš O., Holý P. Pokroky ve vývoji nových antituberkulotik ze skupiny ortokondenzovaných heterocyklických sloučenin. Část 2. Látky obsahující v šestičlenném kruhu více atomů dusíku. Čes. slov. Farm. 2001; 50(5), 211–218.
6. Waisser K., Bureš O., Holý P. Pokroky ve vývoji nových antituberkulotik ze skupiny ortokondenzovaných heterocyklických sloučenin. Část 3. Látky obsahující v šestičlenném kruhu více druhů heteroatomů. Čes. slov. Farm. 2001; 50(6), 267–273.
7. Waisser K., Dražková K. Pokroky ve vývoji amtituberkulotik neobsahujících heteroatomy ve farmakoforu. Část 1. Deriváty karboxylových kyselin. Čes. slov. Farm. 2003; 52(6), 77–81.
8. Waisser K., Dražková K. Pokroky ve vývoji amtituberkulotik neobsahujících heteroatomy ve farmakoforu. Část 2. Ostatmí deriváty kromě karboxylových kyselin. Čes. slov. Farm. 2004; 53(3), 124–130.
9. Waisser K. Vyhodnocování mikrobiologických dat a kvantifikace vztahů mazi strukturou a aktivitou. In: Kohout L., Holý A. (ed.) Chemie a léčiva. Praha: ÚOChB ČSAV 1989; 268–395.
10. Waisser K. Methodic questions of QSAR. III. Quantification of antibacterial activity. Folia Pharmaceutica Univ. Carol. 1992; 16, 39–42.
11. Waisser K. Použití QSAR při vývoji antituberkulotik. Čekoslov. Farm. 1990; 42(5), 223–227.
12. Sriram D., Banerjee D., Varuna T. S. T. V., Sankar M., Yogeeswari P. Novel antirubercular iallyl/dibenzylthiosemicarbazones endowed wirh high activity toward multi-drug resistent tuberculosis. Med. Chem. Res. 2012; 21, 810–815.
13. Bakar R. L., Gattani S. G. Idantification and defelopment of 2,5-disubstituted oxadiazole as potential candidate for treatment of XDR and MDR tuberculosis. Eur. J. Med. Chem. 2012; 47, 278–282.
14. Ahsan M. J., Samy J. G., Jain Ch. B., Dutt K. R., Khalilullah H., Nomani M. S. Discovery of novel anititubercular 1,5-dimethyl-2-phenyl-4-((5-(arylamino)-1,3,4,-oxadiazol-2-yl)methylamino)-1,2-dihydro-3H-pyrazol-3-one analogues. Bioorg. Med. Chem. Letters 2012; 22, 969–972.
15. Klimešová V., Herzigová F., Palát K., Macháček M., Stolaříková J., Dahse H.-M., Möllmann U. The synthesis and antimycobacterial properties of 4-(substitutedbenzylsulfanyl)pyridine-2-carboxamides. ARKIVOC 2012, Part 3, pp. 90–103; http://www. arkat-usa.org/get-file/42667/ (accessed 2012-01-21).
16. Manna K., Agreval K. Potent in vitro and in vivo antirubercular activity of certain newly synthesized indophenazine 1,3,5-trisubstituted pyrazoline derivatives bering benzofuran. Med. Chem. Res. 2011; 20, 300–306.
17. Vavříková E., Polanc S., Kočevar M., Horváti K., Bösze S., Stolaříková J., Vávrová K., Vinšová J. New fluorine-containing hydrazones active against MDR-tuberculosis. Eur. J. Med. Chem. 2011; 46, 4937–4945.
18. Kumar P., Singh A., Snarma U., Singh D., Dobhal M. P., Singh S. Anti-mycobacerial activity of plumericin and isoplumericin agains.t MDR Mycobacterium tuberculosis. Pharmac. Pharmacol. and Therapeutics 2013; 26, 332–335.
19. Krátký M., Vinšová J., Stolaříková J. Antimycobacterial asseamennt of salicylanilide benzoates ikncluding multidrug-resistant tubeculosis strains. Molecules 2012; 17(11), 12812–12820.
20. Vinšová J., Krátký M. Development of new MDR tuberculosis drugs. New York: Nova Biomedical 2010.
Štítky
Farmacie Farmakologie
Článek Nové knihy
Článek vyšel v časopiseČeská a slovenská farmacie
Nejčtenější tento týden
2014 Číslo 1- Využití diklofenaku ve formě gelu v terapii seboroické keratózy
- Kombinace rutosidu a kyseliny askorbové je vysoce účinná v terapii progresivní pigmentové purpury
- Budoucnost guaifenesinu jako OTC myorelaxans
- Příznivý vliv Armolipidu Plus na hladinu cholesterolu a zánětlivé parametry u pacientů s chronickým subklinickým zánětem
-
Všechny články tohoto čísla
-
Kam směřuje vývoj nových antituberkulotik?
Část 2 – Hodnocení in vitro - Produkce flavonoidů a isoflavonoidů v suspenzní kultuře jetele lučního elicitované kyselinou jasmonovou
-
Štúdium lokálnych anestetík: Časť 204*
Determinácia kritických micelových koncentrácií vybraných m-alkoxysubstituovaných pyrolidínoetylesterov kyseliny fenylkarbámovej využitím pyrénu ako sondy - Inhibícia 12/15 lipoxygenázy kurkumínom a extraktom z Curcuma longa L.
- Časopis Česká a slovenská farmacie vstupuje do roku 2014
- Identifikácia a riešenie farmakoterapeutických problémov z pohľadu verejného lekárnika
- Separácia enantiomérov aminokyselín metódou vysokoúčinnej kvapalinovej chromatografie
- Globalizácia a jej dopady v lekárenstve SR
- Docent RNDr. Pavel Komárek, PhD. jubiluje
- 42. konference Syntéza a analýza léčiv byla opět úspěšná
- Nové knihy
-
Kam směřuje vývoj nových antituberkulotik?
- Česká a slovenská farmacie
- Archiv čísel
- Aktuální číslo
- Informace o časopisu
Nejčtenější v tomto čísle- Separácia enantiomérov aminokyselín metódou vysokoúčinnej kvapalinovej chromatografie
- Identifikácia a riešenie farmakoterapeutických problémov z pohľadu verejného lekárnika
- Globalizácia a jej dopady v lekárenstve SR
- Docent RNDr. Pavel Komárek, PhD. jubiluje
Přihlášení#ADS_BOTTOM_SCRIPTS#Zapomenuté hesloZadejte e-mailovou adresu, se kterou jste vytvářel(a) účet, budou Vám na ni zaslány informace k nastavení nového hesla.
- Vzdělávání



